《化工設備設計全書》系列一直以來都是化工人的必備經典書籍之一,雖然有些老,但,經典之作,永不過時。
今天,小編我特意從網絡搜集到全系列書籍,整理出來供大家下載學習,大家按自己的需要,可選擇一些對自己適合的進行學習。全系列一共15本,本次分享全部包含在內,具體目錄如下:

后臺回復關鍵字:【15】 領取共15本《化工設備設計全書》全套書籍
濕法和干法脫硫是目前2大主要脫硫方法,他們之間的區別主要是通過以下幾個方面來實現:干法脫硫與濕法脫硫的區別 濕法和干法脫硫是目前2大主要脫硫方法,他們之間的區別主要是通過以下幾個方面來實現。
一、干法煙氣脫硫
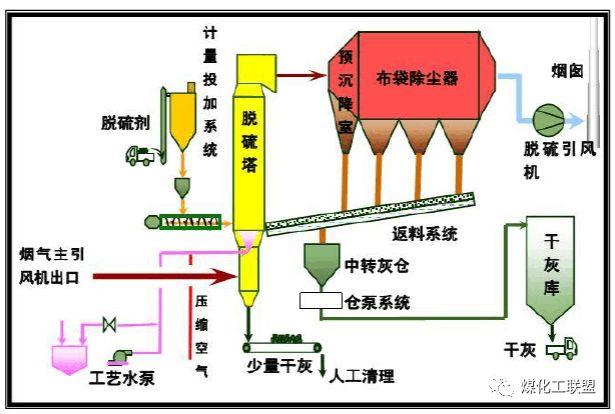
干法煙氣脫硫是指應用粉狀或粒狀吸收劑、吸附劑或催化劑來脫除煙氣中的SO2。它的優點是工藝過程簡單,無污水、污酸處理問題,能耗低,特別是凈化后煙氣溫度較高,有利于煙囪排氣擴散,不會產生“白煙”現象,凈化后的煙氣不需要二次加熱,腐蝕性小;其缺點是脫硫效率較低,設備龐大、投資大、占地面積大,操作技術要求高。主要的方法有:
吸著劑噴射法按所用吸著劑不同分為鈣基和鈉基工藝,吸著劑可以干態,濕潤態或漿液,噴入部位可以為爐膛、省煤器和煙道。鈣硫比為2時,干法工藝的脫硫效率達50%~70%,鈣的利用率達50%,這種方法較適合老電廠改造,因為在電廠排煙流程中不需增加任何設備就能達到脫硫目的。
接觸氧化法此法與工業制酸法一樣,是以硅石為載體,以五氧化二釩或硫酸鉀為催化劑,使SO2氧化成SO3。SO3與水汽作用形成硫酸或與氨作用生成(NH4)2SO4。此法是高溫操作,所需費用高,但由于技術上較為成熟,目前國內外對高濃度煙氣的治理多采用此法。
電子束輻照法本法的工藝技術簡單,它是利用高能電子束的光化學反應,用氨作為吸收劑。煙氣通過輻照反應器,經輻照后,分解產生了大量的氫氧基和氧原子,促進煙氣中二氧化硫和氮氧化物形成硫酸和硝酸,繼而與添加物氨反應生成硫酸銨、硝酸銨等混合物,作為農用肥料。
二、濕法煙氣脫硫
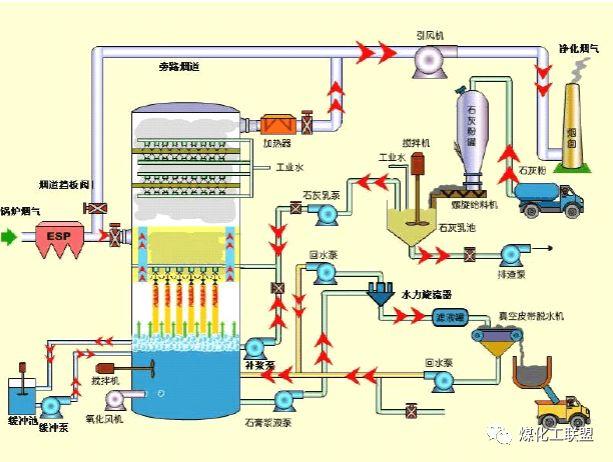
濕法煙氣脫硫是指應用液體吸收劑(如水或堿性溶液等)洗滌煙氣脫除煙氣中的SO2。它的優點是脫硫效率高,設備小、投資省、操作較容易、容易控制以及占地面積小;而缺點是易造成二次污染,存在廢水后處理問題,能耗高,特別是洗滌后煙氣的溫度低,不利于煙囪排氣的擴散,易產生“白煙”,需要二次加熱,腐蝕嚴重等。主要的方法有:
石灰石-石膏法該工藝是利用石灰石/石灰石漿液洗滌煙道氣,使之與SO2反應,生成亞硫酸鈣(CaSO3),經分離的亞硫酸鈣可以拋棄,也可以通入空氣強制氧化和加入一些添加劑,以石膏形式進行回收。為了減輕SO2洗滌設備的負荷,先要將煙道氣除塵,然后再進入除塵設備與吸收液發生反應。石灰/石灰石-石膏法技術比較成熟,吸收劑價廉易得,運行可靠,應用最廣,脫硫效率可達90%以上。
鈉法此法是用氫氧化鈉、碳酸鈉、或亞硫酸鈉溶液為吸收劑吸收煙氣中的SO2,因該法具有對SO2吸收速度快,管路和設備不易堵塞等優點,所以應用比較廣泛,吸收液可以經無害化處理后棄去或適當方法處理后獲得副產品NaSO3晶體、石膏、硫酸等。
鎂法此法具有代表性的工藝有西德WilhlmGrillo公司發明的基里洛法和美國ChemicalConstructionCo發明的凱米克法。
基里洛法是用吸收性能好并容易再生的MgxMnOy為吸收劑吸收煙氣中的SO2,此法所得副產物H2SO4的濃度可達98%。凱米克法又稱氧化鎂法,用串聯兩個文丘里除塵器除去煙氣中微小的塵粒,并用MgO溶液吸收煙氣中的SO2。吸收過程中生成的MgSO4·7H2O和MgSO4·6H2O的晶體與焦碳一起在1000℃下加熱分解得到SO2和MgO。再生的MgO可重新用作吸收劑。
氨法此法是用氨水為吸收劑吸收煙氣中的SO2,其中間產物為亞硫酸銨和亞硫酸氫銨,采用不同方法處理中間產物可回收硫酸銨、石膏、單體硫等副產品。
磷銨復肥法該法是利用天然磷礦石和氨為原料,在煙氣脫硫過程中副產品為磷銨復合肥料,工藝流程主要包括四個過程,即:活性炭一級脫硫并制得稀硫酸;稀硫酸萃取磷礦制得稀硫酸溶液;磷酸和氨的中和液[(NH4)2HPO4]二級脫硫;料漿濃縮干燥制磷銨復肥。脫硫效率為95%以上。
通過以上分析我們知道濕法脫硫主要的優點就是運行費用比較低,效率高,但是比較耗水。干法脫硫的優化是不消耗水資源,但是脫硫效率不是很理想。這個要根據具體情況來掌握使用哪種脫硫方法。






